Ce chapitre est issu de l'ouvrage "29 notions clefs pour savourer et faire savourer la science - primaire et collège", paru aux éditions Le Pommier en août 2009.
Les états de l'eau
Type de ressources
Thème(s) Scientifique(s) 1er degré
Crédits

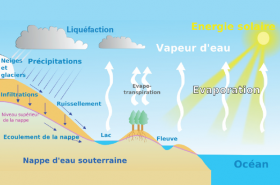
L’eau est très présente sur la Terre. Elle couvre environ 70 % de sa surface, sous forme d’océans (97,8 %), de rivières et de lacs (0,006 %), de glaces polaires (1,74 %) et de nappes souterraines. On en trouve aussi dans les nuages. Pourtant l’eau est un corps dont le comportement est exceptionnel et elle recèle encore nombre de mystères…
Vous souhaitez aborder ce sujet avec vos élèves ?
Consultez nos ressources pour la classe !